Succesvolle biggenvaccinatie begint met de juiste timing!

Immuniteit bouwt niet direct op
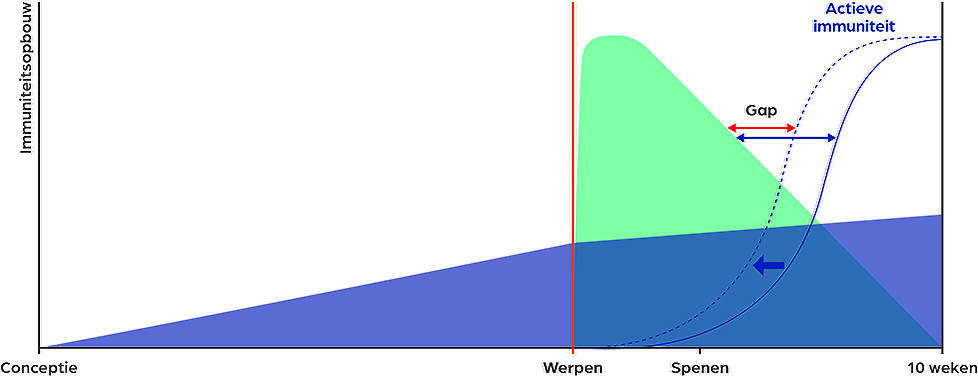
Na vaccinatie heeft een big tijd nodig om bescherming op te bouwen. Deze zogenoemde onset of immunity varieert per vaccin en pathogeen, maar bedraagt doorgaans één tot enkele weken. Bovendien kan de aanwezigheid van maternale antistoffen de respons op vaccinatie beïnvloeden.3,5
Tegelijkertijd daalt in de eerste levensweken de maternale immuniteit die met de biest wordt opgenomen. Rond de speenleeftijd ontstaat daardoor een kritische overgangsfase: de passieve bescherming neemt af, terwijl de actieve immuniteit nog in ontwikkeling kan zijn. Wanneer vaccinatie te laat plaatsvindt, kan een ‘immunologisch gat’ ontstaan. De snelheid waarmee maternale antistoffen dalen verschilt per bedrijf en zelfs per toom. Biestopname, zeugenvaccinatieschema’s, infectiedruk en bedrijfsstatus spelen hierbij een bepalende rol. Vaccinatieplanning is daarom per definitie maatwerk.
Wat ziet u terug in uw cijfers?
Wanneer bescherming niet tijdig op niveau is, vertaalt zich dat doorgaans rechtstreeks in de technische resultaten:
- meer hoest en longschade
- lagere dagelijkse groei
- hogere voederconversie
- meer antibioticagebruik
- verhoogde uitval in de eerste weken na opleg
Een suboptimale timing van vaccinatie manifesteert zich dus niet alleen klinisch, maar ook economisch.
Verschillen tussen belangrijke infecties
Niet elke ziekteverwekker vraagt om dezelfde vaccinatiestrategie of timing.
PCV2
Porcine circovirus type 2 (PCV2) kan al op jonge leeftijd subklinisch circuleren. Vroege vaccinatie vóór natuurlijke veldinfectie vermindert de virale belasting, klinische verschijnselen en productieverliezen.4,5
Het moment van vaccineren kan best afgestemd worden op de mate van aanwezigheid van maternale antistoffen en verwachte infectieleeftijd.
PRRS
PRRS-virus kent een complexe interactie met het immuunsysteem en veroorzaakt zowel respiratoire als reproductieve problemen. De bedrijfsstatus, de circulerende veldstammen en de stabiliteit van de zeugenstapel bepalen mede de vaccinatiestrategie.1
Omdat verspreiding vaak samenvalt met stressmomenten zoals mengen of verplaatsen, is tijdige bescherming cruciaal voor bedrijfsstabilisatie.
Mycoplasma hyopneumoniae (M. hyo)
M. hyo veroorzaakt chronische longlaesies en groeivertraging. Besmetting rondom het spenen zijn sterk gerelateerd aan longetsels bij de slacht. Vaccinatie reduceert longschade en uitscheiding, maar de immuniteitsopbouw verloopt geleidelijk.2 Overweeg een vroege vaccinatie van de biggen (in de eerste levensweek), wanneer er bij onderzoek een vroege mycoplasma infectie op het bedrijf voorkomt.
Actinobacillus pleuropneumoniae (App)
App veroorzaakt vaak acute uitbraken na stressmomenten. Omdat maternale antistoffen de eerste levensweken nog actief bescherming bieden, maar ook vaccinrespons kunnen neutraliseren, is timing cruciaal. Daarom worden biggen in de praktijk veelal vanaf 6 weken leeftijd of ouder gevaccineerd, wanneer de maternale immuniteit voldoende is gedaald voor een optimale opbouw van actieve bescherming.
Vaccineren vóór de piek in infectiedruk
Wanneer vaccinatie plaatsvindt rond of na het spenen, kan de immuniteitsopbouw samenvallen met een stijgende infectiedruk. In dat geval loopt de bescherming achter op wat er in de stal gebeurt.
De optimale timing hangt af van meerdere factoren:
- speenleeftijd
- infectiedruk op het bedrijf
- zeugenvaccinatieschema
- biestmanagement
- technische resultaten
Analyse van gezondheidsdata, longscoringsresultaten en serologie helpt om het optimale vaccinatiemoment af te stemmen op het moment waarop bescherming daadwerkelijk nodig is. Vaccinatieplanning is daarmee geen vast protocol, maar een dynamisch onderdeel van het bedrijfsgezondheidsplan.
De praktische vraag is dan ook:
Sluit het huidige vaccinatiemoment aan bij het moment waarop de infectiedruk daadwerkelijk toeneemt. Bespreek dit samen met uw dierenarts. In de speenperiode ziet u het verschil tussen ‘gevaccineerd’ en ‘op tijd beschermd’ vaak direct terug in uw technische resultaten.
Referenties
1. Lunney, J. K., Benfield, D. A., & Rowland, R. R. R. (2016). Porcine reproductive and respiratory syndrome virus: An update on an emerging and re-emerging viral disease of swine. Virus Research, 226, 1–6.
2. Maes, D., Segalés, J., Meyns, T., Sibila, M., Pieters, M., & Haesebrouck, F. (2008). Control of Mycoplasma hyopneumoniae infections in pigs. Veterinary Microbiology, 126(4), 297–309.
3. Martínez-Boixaderas, N., Sibila, M., et al.(2022). Impact of maternally derived immunity on immune responses elicited by piglet early vaccination against common porcine respiratory pathogens. Porcine Health Management, 8, Article 17.
4. Opriessnig, T., Meng, X. J., & Halbur, P. G. (2007). Porcine circovirus type 2-associated disease: Update on terminology, clinical manifestations, pathogenesis, diagnosis, and intervention strategies. Journal of Veterinary Diagnostic Investigation, 19(6), 591–615.
5. Poulsen, B., Van Vlaenderen, I., et al.(2021). Do high levels of maternally derived antibodies interfere with piglet vaccination against porcine circovirus type 2? Vaccines, 9(8), 923.
MM-46460